Trattamento semplificato di un’atrofia ossea combinata del mascellare superiore, associata ad una lesione endoparodontale con deiscenza del pavimento sinusale in sede 1.4-1.5, ed a una perimplantite in sede 1.7
F
45 anni
Paziente ASA 2
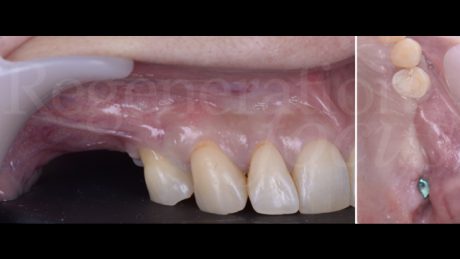
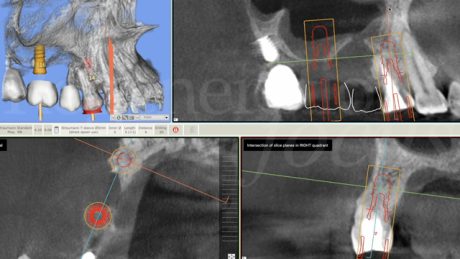
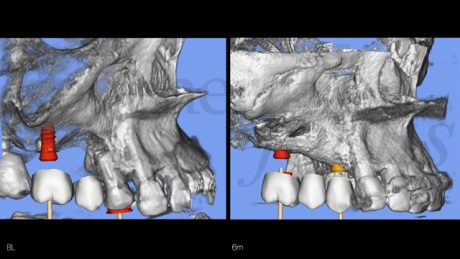
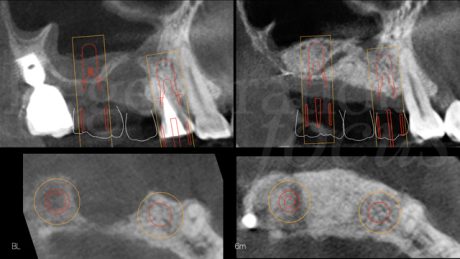
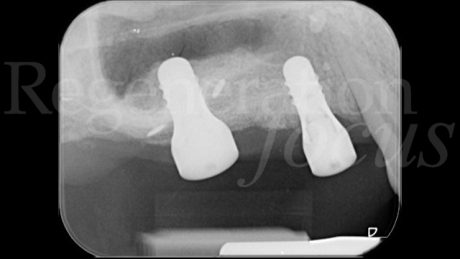
Presenza di un'atrofia ossea verticale nella cresta ossea edentula 1.5 associata a una deiscenza del pavimento sinusale sul fondo del difetto, e la presenza di una perimplantite severa a livello dell'impianto 1.7. Si riscontra inoltre una pneumatizzazione del seno mascellare destro in sede 1.6, con un’altezza ossea residua di ca. 1,5 mm.
Necessità di ripristinare la profondità del fornice vestibolare e d un'idonea anatomia dei tessuti molli perimplantari.
Buona
Richiesta di una riabilitazione protesica fissa del primo sestante parzialmente edentulo
Introduzione
I difetti ossei dei mascellari derivanti dai processi riassorbitivi che seguono all’estrazione di un elemento dentale, all’edentulia di lunga durata, alla parodontite, o a traumi, sono un reperto comune nei pazienti parzialmente o totalmente edentuli che richiedono una riabilitazione protesica implanto-supportata (Benich & Hammerle 2014). In presenza di atrofie orizzontali complesse ed atrofie verticali, le tecniche ricostruttive maggiormente documentate per il ripristino di un volume osseo tridimensionale compatibile con l’inserimento di impianti dentali in posizione protesicamente guidata, si basano sull’uso di osso autologo in blocchi o particolato, in virtù del suo potenziale osteogenetico, osteoinduttivo ed osteoconduttivo, e sull’utilizzo di dispositivi rigidi per il mantenimento dello spazio rigenerativo, quali blocchi/lamine ossee, membrane rinforzate o mesh in titanio (Sanz-Sánchez et al. 2018; Urban et al. 2023). Tuttavia, tali tecnologie rigenerative si sono rivelate estremamente operatore-sensibili, in seguito al riscontro di tassi di complicanze molto variabili (da 0 a 45% – Rocchietta et al. 2008), nonché associate ad una maggior morbilità post-chirurgica, soprattutto quando abbinate all’utilizzo di osso autologo prelevato in sede orale o extra-orale (Chiapasco et al. 2018).
Obiettivi
Scopo del presente case report è quello di descrivere l’utilizzo di una nuova tecnologia rigenerativa basata sull’uso di un gel viscoelastico a base polinucleotidi associati a acido ialuronico (Regenfast®, Officine Biofarmaceutiche Mastelli, Sanremo, Italia), applicato con una tecnica stratificata, nel trattamento ricostruttivo di un’atrofia ossea mascellare a scopo peri-implantare.
Descrizione del Caso
Una paziente di 45 anni, fumatrice (10/die), in buono stato di salute generale, si presenta richiedendo una riabilitazione protesica fissa del primo sestante parzialmente edentulo. L’anamnesi odontoiatrica rileva un pregresso fallimento implantare in sede 1.5, secondario a perimplantite, con sviluppo di una comunicazione oro-antrale in seguito all’estrazione dell’impianto, chiusa mediante un lembo di Rehrmann sostenuto da un avanzamento coronale della bolla di Bichat. È inoltre presente un elemento 1.4 affetto da una lesione endo-parodontale di terzo grado, già trattato con terapia endodontica e, successivamente mediante endodonzia chirurgica. All’esame clinico e radiografico, si riscontra la persistenza della lesione endo-parodontale in sede 1.4, la presenza di un’atrofia ossea verticale nella cresta ossea edentula 1.5 associata a una deiscenza del pavimento sinusale sul fondo del difetto, e la presenza di una perimplantite severa a livello dell’impianto 1.7. Si riscontra inoltre una pneumatizzazione del seno mascellare destro in sede 1.6, con un’altezza ossea residua di ca. 1,5 mm. Eseguita la ceratura digitale del caso e riscontrata la presenza di una quota ossea residua incompatibile con l’inserimento di impianti in posizione protesicamente guidata, si progetta un intervento combinato di:
a) Estrazione del dente 1.4 e dell’impianto 1.7
b) Rialzo del seno mascellare con approccio laterale in sede 1.6
c) Rigenerazione ossea con tecnica GBR in sede 1.5 ed 1.4.
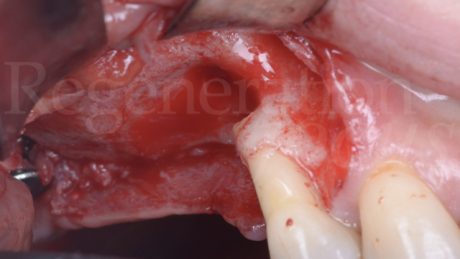
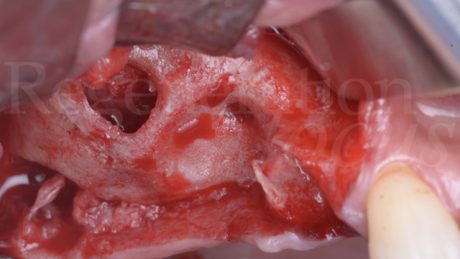
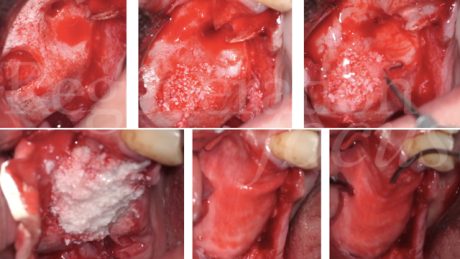
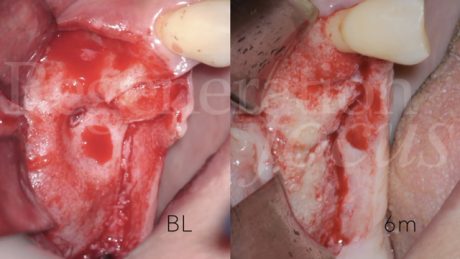
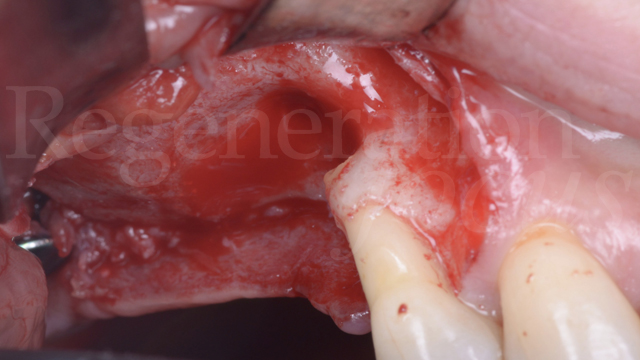
Pertanto, in anestesia locale, si esegue un’incisione a busta in sede 1.8-1.4 con scarico mesiale, si scheletrizza il mascellare superiore isolando per via smussa la deiscenza del pavimento sinusale in sede 1.5, e si procede all’estrazione del dente 1.4 e dell’impianto 1.7 ed alla degranulazione dei difetti post-estrattivi.
Segue pertanto una opercolizzazione ossea in sede 1.6, con scollamento della membrana di Schneider e creazione di uno spazio subsinusale esteso fino alla deiscenza in 1.5. Segue quindi un primo apporto di Regenfast® sul letto osseo ricevente ed il riempimento dello spazio subsinusale con Geistlich Bio-Oss® granulometria small.
Segue la stabilizzazione vestibolare di una membrana Geistlich Bio-Gide® con pins in titanio, ed il posizionamento di Geistlich Bio-Oss® a ricostruzione del difetto in sede 1.5 ed 1.4.
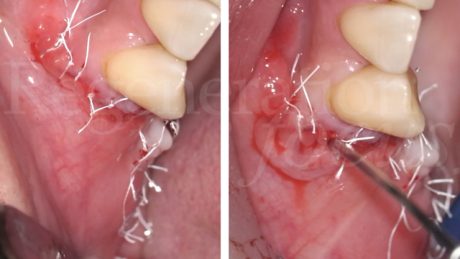
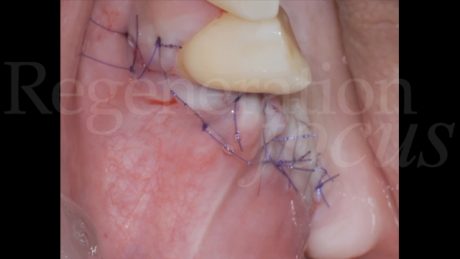
La membrana viene quindi ribattuta sull’aspetto palatale della cresta, e stabilizzata con una combinazione di pin in titanio e suture a materassaio palatali. La procedura termina con il rilascio del lembo vestibolare, una seconda applicazione di Regenfast® sulla superficie della membrana stabilizzata, la chiusura dei lembi per prima intenzione mediante una combinazione di punti a materassaio interno e punti staccati, ed una terza applicazione di Regenfast® al di sopra della linea di chiusura.
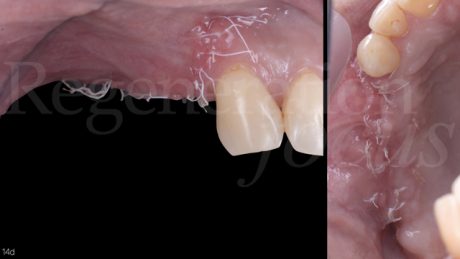
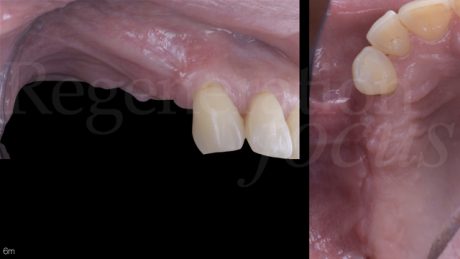
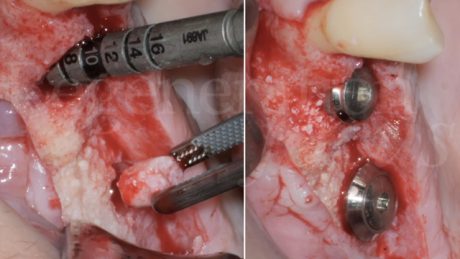
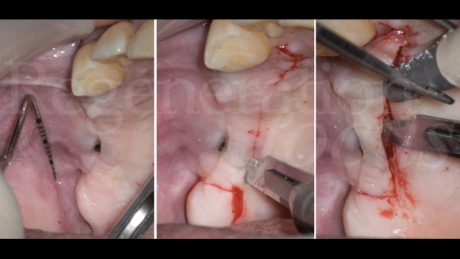
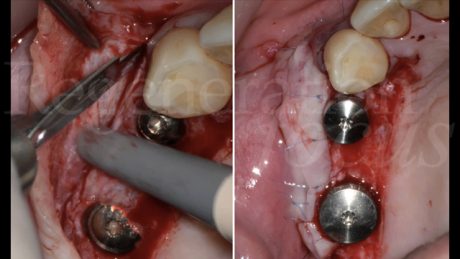
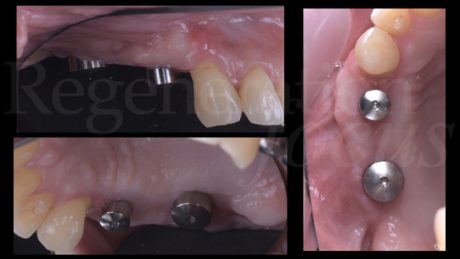
Dimessa la paziente in stato vigile e orientato, con coagulo competente, si rimuove la sutura a distanza di 14 giorni, riscontrando un decorso post-chirurgico nella norma. A distanza di 6 mesi, previa acquisizione di una CBCT, si procede con il rientro chirurgico nella sede ricostruita. Scheletrizzato il mascellare ricostruito, si riscontra una parziale risoluzione del difetto verticale in sede 1.5 ed il ripristino di volumi ossei idonei all’inserimento di impianti in posizione protesicamente guidata in sede 1.4 ed 1.6. Durante la preparazione dei letti implantari, si esegue il prelievo di due carote ossee mediante fresa trephine da 3.3 mm. Segue quindi l’inserimento di due impianti Tissue Level SP 4.1x8mm (Straumann Institute AG) e l’adozione di un protocollo di guarigione sommerso. A distanza di 3 mesi, si procede alla seconda fase implantare abbinata ad una vestiboloplastica, col fine di ripristinare la profondità del fornice vestibolare ed un’idonea anatomia dei tessuti molli perimplantari. Le biopsie del tessuto osseo prelevate in fase di inserimento implantare sono state processate con tecnica standard, non decalcificata, e colorate con blu di toluidina e pironina gialla.
Risultati
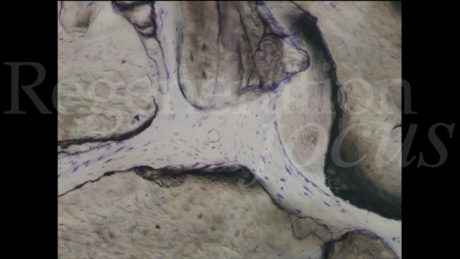
A 9 mesi dalla chirurgia ricostruttiva, si riscontra una buona stabilità dei tessuti duri e molli perimplantari. All’esame istologico descrittivo (Fig. 18) si riscontrano granuli residui del biomateriale utilizzato per la rigenerazione, a stretto contatto col tessuto osso neoformato. Cellule simil-osteoblastiche sembrano allineate lungo il fronte di rigenerazione ossea. Gli spazi midollari appaiono ricchi di vasi e privi di infiltrato infiammatorio.
Conclusioni
L’utilizzo di una strategia rigenerativa semplificata, che integri tecnologie di mantenimento di spazio riassorbibili assieme a booster biologici, potrebbe rappresentare una valida alternativa per il trattamento di atrofie ossee incompatibili con l’inserimento di impianti osteointegrati in posizione protesicamente guidata.
Analisi istologica a cura della Prof. Claudia Dellavia e Dr.ssa Gaia Pellegrini, Laboratorio Sezioni sottili, Dipartimento di Scienze Biomediche Chirurgiche e Odontoiatriche, UNIMI.
Per i dettagli della chirurgia è disponibile il video chirurgico “GBR e rialzo del seno in presenza di un’atrofia ossea verticale e orizzontale, associata ad una lesione endoparodontale con deiscenza del pavimento sinusale in sede 1.4, ed a una perimplantite in sede 1.7”
Re-live Surgeries

Geistlich Biomaterials Italia S.r.l.
Via Castelletto 28, 36016 Thiene (VI)
Tel: +39 0445 370 890
Fax: +39 0445 370 433
Mail: [email protected]
Regeneration Focus è il primo portale in Italia dedicato alla rigenerazione ossea e tissutale nel campo dentale e maxillo-facciale, ideato e supportato da Geistlich Biomaterials nel 2012, oggi diventato il portale education sulla rigenerazione dei tessuti duri e molli.
Vi invitiamo a leggere, esplorare e divertirvi a scegliere la modalità di formazione che più fa per voi.